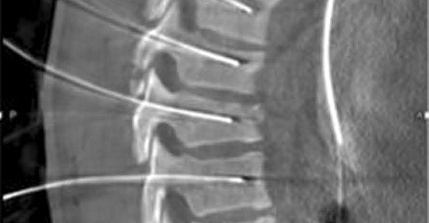
Применение стволовых клеток в спинальной хирургии
Лечение заболеваний позвоночника с помощью стволовых клеток становится все более реальным. Последние достижения науки позволяют исследователям и спинальным хирургам изучать способность стволовых клеток к восстановлению изношенных межпозвоночных дисков, повреждений спинного мозга и активизировать рост костной ткани при спондилодезе. Oбзор последних достижений в этой области был опубликован специалистами центра спинальной хирургии клиники "Хадасса" (руководитель - доктор Леон Каплан) в журнале World Journal of Stem Cells
Последние годы стволовые клетки находятся в центре внимания регенеративной медицины. Региональные стволовые клетки, взятые непосредственно из костного мозга, жировой ткани или крови способны как к митозу, так и мультипотентной дифференциации в различные типы клеток. Стволовые клетки используются для замещения или восстановления поврежденных тканей путем их дифференциации в клетки, ускоряющие процесс заживления или непосредственно реконструирующие ткани.
Несмотря на многолетние исследования природы стволовых клеток и процесса дифференциации, их приживаемость, наряду с биохимическим и физиологическим мониторингом состояния пациента при трансплантации до сих пор остается трудной задачей. Благодаря достижениям естественных наук осуществляется моделирование пространственной организации клеток (скаффолд-технологии), которые одновременно позволяют удерживать клетки в области трансплантации и проникать нутриентам для поддержания жизнестойкости клеток. Достижения генной инженерии позволяют модифицировать стволовые клетки, чтобы вызвать экспрессию селективного фактора роста и ускорить восстановление тканей.
Некоторые задачи спинальной хирургии рассматривались в ходе экспериментальной терапии с использованием стволовых клеток. Изучалась возможность лечения дегенеративных заболеваний позвоночника, таких, как остеохондроз, путем биологического восстановления межпозвоночных дисков с помощью различных типов стволовых клеток и факторов роста, в попытке снизить необходимость хирургического вмешательства.
С помощью трансплантации стволовых клеток могут быть ослаблены возможные тяжелые последствия повреждений спинного мозга путем восстановления нейронов. Тканевая инженерия занимается разработкой новых методов для нужд спинальной хирургии, главным образом, для сращивания костей и достижения стабилизации позвоночника при спондилодезе. Также многие исследователи работают над тем, чтобы ятрогенные повреждения периферических нервов и окружающих позвоночник скелетных мышц, которые могут возникнуть в ходе операции, когда подготавливается доступ к позвоночнику, были бы столь не драматичны в долгосрочной перспективе для двигательной способности пациента. В целом, несмотря на то, что лечение стволовыми клетками находится на стадии исследований, оно предоставляет многообещающие возможности в лечении заболеваний позвоночника, а также снижении рисков в спинальной хирургии.
Применение стволовых клеток в спинальной хирургии.
Спондилодез.
Операция спондилодеза проводится для устранения боли, деформаций или неврологических расстройств, вызванных дегенеративными заболеваниями, спинальными опухолями, переломами и деформациями позвоночника (сколиоз, кифоз и др.). Сращивание двух и более позвонков помогает устранить боль, связанную с нарушенным взаимодействием позвонков при смещении.
Частота проведения спондилодеза поясничного отдела позвоночника с 1990 г. выросла на 220 %. Этот показатель больше, чем для аналогичный для артропластики коленного сустава и тазобедренного сустава вместе взятых. Амбулаторная хирургия поясничного отдела позвоночника также имеет тенденцию к более широкому применению по сравнению со стационарной хирургией. Частота применения спондилодеза шейного и грудо-поясничного отделов позвоночника увеличилась на 89 и 31% соответственно. На сегодняшний день, внедрение новых технологий в хирургию не гарантирует снижение частоты повторных операций. Для успешного сращивания костей необходимы следующие условия: достаточное количество клеток, формирующих костную ткань (остеогенез), особая микросреда, способствующая синтезу костного материала при помощи различных факторов роста (остеоиндукция), а также каркас или кейдж (имплантат), который обеспечивает надежную базу для костного роста (остеокондукция).
Несмотря на последние достижения в моделировании имплантируемых каркасов и улучшенные материалы для спондилодеза, псевдоартроз остается актуальной проблемой для 13 - 41.1% пациентов. Факторы риска псевдоартроза включают пожилой возраст, пояснично-грудной кифоз (искривление верхнего отдела позвоночника), курение, сахарный диабет, нарушение метаболизма костной ткани. К заболеванию более предрасположены женщины. Пациенты в возрастной группе от 60-ти лет все чаще нуждаются в спондилодезе, поэтому медицинское сообщество активно разрабатывает альтернативное лечение, направленное на рост костной ткани и сращивание костей, в том числе при помощи имплантации стволовых клеток.
Традиционно для сращивания костей используется аутологическая трансплантация костного мозга из подвздошной кости, однако этот процесс чреват осложнениями. Аллогенная трансплантация (от донора) или трансплантация синтетического материала сохраняет остеокондуктивные и, в различной степени, остеоиндуктивные свойства, однако при этом не возникают клетки, необходимые для соединения костей.
Установлено, что мезенхимальные стволовые клетки (МСК), взятые из костного мозга, жировой ткани, надкостницы или скелетных мышц способны дифференцироваться в остеобласты как внутри организма, так и вне его. Стволовые клетки жировой ткани (СКЖТ) менее других используются в экспериментальных моделях, однако являются мультипотентными, т.е. могут дифференцироваться в адипоциты, остеобласты, хондроциты или миоциты, если выращены в правильной микросреде. Клетки обоих типов продемонстрировали значительную эффективность в сращивании костей при различных условиях культивирования клеток, имплантации каркаса и введения факторов роста.
Костный морфогенетический белок -2 (BMP - bone morphogenetic protein) представляет собой фактор роста, который все чаще применяется при спондилодезе, однако вне зарегистрированных показаний, что может приводить к различным осложнениям. По результатам экспериментов, генетически модифицированные МСК, разработанные для экспрессирования BMP-2, способствуют спондилодезу у мышей после инъекции в параспинальную мускулатуру в той же степени, что и инструментальный метод.
Для решения проблемы осложнений, Т. С. Фу с коллегами исследовали способность небольшого количества BMP-2 в соединении с МСК давать приемлемый эффект в сращивании костей. Исследователи обнаружили, что экспериментальная группа кроликов, которым вводили МСК, помещенный в альгинат с небольшим количеством BMP-2, достигла того же результата в сращивании костей, что и группа, для лечения которой применялась аутогенная трансплантация из подвздошной кости. Дополнительным свидетельством того, что МСК могут заменить аутогенную трансплантацию или BMP-2 служит снижение количества осложнений в группе с терапией МСК по сравнению с группой BMP-2.
Х. С. Сео предпринял попытку повысить сращиваемость костей в экспериментах над мышами путем трансплантации МСК, помещенных в гидроксиапатит в дополнение к фактору роста фибробластов-4, однако обнаружил, что группа без дополнительного фактора роста достигла более высокой сращиваемости костей.
Помимо выбора подходящего фактора роста, роль играет интенсивность остеогенной дифференциации клеток. По результатам одного исследования, спондилодез у кроликов проходит успешно в 80 % случаев с помощью МСК, выращенных в остеогенной дифференцированной среде и только в 33 %, если клетки были выращены вне дифференцированной среды. Если МСК трансплантировались без изменений условий выращивания, дополнительных разработок генной инженерии или факторов роста, то эффективность процедуры снижалась в различных экспериментах с животными, где в качестве материала для трансплантата использовался бета-трикальцийфосфат или пористая керамика.
В последнее время в тканевой инженерии широко применяются стволовые клетки, полученные из жировой ткани, отчасти из-за легкости их отбора в ходе липосакции. Эффективность СКЖТ, экспрессирующих костный морфогенетический белок (BMP), в спондилодезе была доказана на животных с нарушением метаболизма костной ткани. В ходе исследования по сравнению МСК и СКЖТ, экспрессирующих BMP-2, сращиваемость костей у мышей в обеих группах была удовлетворительной и не имела значительных отличий. Более пристальное внимание к использованию СКЖТ в спондилодезе обусловлено относительной легкостью получения этих клеток из организма пациента. В целом же применение стволовых клеток ограничено тем количеством, которое можно получить при липосакции или спинномозговой пункции. Для увеличения популяции плюрипотентных клеток необходимо их размножение in vitro (в лабораторных условиях).
Восстановление межпозвоночных дисков
Дегенеративное заболевание позвоночника возникает в результате сложного биомеханического процесса и молекулярных изменений в межпозвоночном диске. Здоровый диск состоит из пульпозного ядра, практически полностью состоящего из коллагеновых волокон II типа с высоким содержанием протеогликана и аггрекана, которые отвечают за сопротивление деформации. Пульпозное ядро диска окружает фиброзное кольцо, состоящее из коллагеновых волокон I типа, спирально закрученных вокруг межпозвоночного диска. Коллагеновые волокна выполняют функцию амортизатора при деформациях сгибания и скручивания.
Здоровый межпозвоночный диск лишен нервов и сосудов в связи с высоким содержанием протеогликана в пульпозном ядре и получает большую часть питательных веществ путем диффузии через хрящевую замыкательную пластинку. Прогрессирующая кальцификация замыкательной пластинки, начавшись в юном возрасте, может привести к уменьшению количества питательных веществ, поступающих к диску. Предположительно это приводит к фенотипическим изменением диска и, как следствие, снижению синтеза протеогликанов и коллагена II типа, а также повышению синтеза коллагена I и III типов и увеличению активности матриксных металлопротеиназ.
В большинстве случаев изменения биохимического состава диска вызывают значительные изменения морфологии, в том числе уменьшение толщины диска, что может привести к защемлению нервов. Боль в нижней части спины является клиническим проявлением дегенеративного заболевания позвоночника и устраняется, как правило, консервативными методами: корректированием образа жизни или трудовой деятельности, физиотерапией, болеутоляющими препаратами, акупунктурой и эпидуральными инъекциями.
При устойчивых симптомах, которые вызывают прогрессирующую деформацию позвоночника или неврологические нарушения, показано хирургическое лечение путем замены межпозвоночного диска или спондилодез. Применение факторов роста, антагонистов воспалительных цитокинов и внутриклеточных регуляторных белков доказало свою эффективность в восстановлении клеток пульпозного ядра как in vitro, так и in vivo.
Эффективность данных методов в клинической практике ограничена скоростью дегенерации молекул лечебного вещества в организме. Генная терапия, несмотря на успешное применении на животных моделях, имеет значительный риск, связанный с вектором (переносчиком) генов. Лечение дегенеративного заболевания позвоночника при помощи стволовых клеток основано на реконструкции матрикса пульпозного ядра. Исследователи Нишимура и Мочида первыми осуществили реимплантацию аутологичных клеток пульпозного ядра для экспериментального лечения грыжи у крыс и сообщили об уменьшении дегенерации фиброзного кольца и замыкательной пластинки, а также сохранении пульпозного ядра по сравнению с контрольной группой.
В настоящее время не доказана способность МСК дифференцироваться в клетки пульпозного ядра, способные продуцировать протеогликан, т.к. точный фенотип этих клеток еще не определен. Однако исследования показали, что различные стимуляторы среды и генетические манипуляции могут вызвать дифференциацию МСК в клетки, подобные клеткам пульпозного ядра. Ричарсдсон с коллегами трансфицировали МСК с помощью фактора транскрипции SOX-9 и обнаружили, что они дифференцируются в клетки, подобные хондроцитам, с выделением маркеров пульпозного ядра – коллагена II типа и аггрекана. Рисбуд с коллегами культивировали иммобилизованные стволовые клетки в гипоксических условиях с трансформирующим фактором роста бета и обнаружили, что такие условия стимулируют дифференциацию МСК в клетки, подобные клеткам пульпозного ядра.
Подобная дифференциация стволовых клеток в клетки, экспрессирующие фенотипические маркеры пульпозного ядра наблюдалась и в ходе экспериментов с кроликами. Сакай с коллегами исследовали эффект трансплантации МСК в здоровый и в дегенерированный межпозвоночный диск. Ученые обнаружили, что имплантированные клетки дифференцируются в клетки подобные тем, что составляют пульпозное ядро, вырабатывающие коллаген II типа и протеогликан, при этом не причиняя вреда организму кроликов. У дегенеративных дисков наблюдалось увеличение толщины и улучшение гидратации. Аллогенные МСК экспериментально трансплантировались в межпозвоночные диски мышей и показали благоприятную приживаемостью и распространение.
Однако проблемы, связанные с иммунной реакцией человека на аллогенные стволовые клетки, ограничивают их клиническое использование. Группа исследователей во главе с Орозко провели трансплантацию аутологичных МСК десяти пациентам с дегенеративным заболеванием позвоночника. Они обнаружили значительное снижение боли и увеличение подвижности после 3 месяцев терапии. Данное исследование было достаточно ограничено по возрасту пациентов (в среднем 35 лет) и их количеству (10 человек). Полученные результаты при этом подтверждают необходимость проведения более масштабных клинических испытаний, чтобы облегчить внедрение стволовых клеток в клиническую практику для лечения пациентов, страдающих от дегенеративного заболевания позвоночника.
Повреждения спинного мозга
Повреждения спинного мозга (ПСМ) - это поражения спинного мозга в результате травмы, которые могут приводить к серьезным последствиям вплоть до смерти. Наиболее частыми причинами травматических ПСМ являются дорожно-транспортные происшествия, спортивные, бытовые и производственные травмы. Каждый год насчитывается 15-40 случаев ПСМ на миллион человек, при этом большинство пострадавших – мужчины от 16 до 30 лет. ПСМ включает несколько комплексных стадий, которые до сих пор изучаются на молекулярном уровне.
Первичная или острая стадия включает механическое повреждение и ушиб нервов и тканей, окружающих спинной мозг. Интенсивность травматического повреждения прямо пропорциональна количеству погибших клеток. Как следствие, спинной мозг опухает и происходит блокировка кровотока, зачастую одновременно с кровотечением, что приводит к гипоксии.
Для вторичной или подострой стадии ПСМ характерны перекрывающие друг друга фазы длительного воспаления, оксидативного стресса и иммунных реакций. Повышение уровня глутамата в крови, образование активных форм кислорода и чрезмерная липопероксидация приводят к обширной смерти нейронов и глиальных клеток, а также аксональной дегенерации.
Рубцовая ткань, образующаяся в ходе третье (хронической) стадии, формирует физический и биохимический барьер для аксональной регенерации, что осложняет процесс восстановления.
В рамках исследования ученые проводили трансплантацию стволовых клеток, в надежде, что данный метод ускорит функциональную реабилитацию пациентов поле ПСМ. Процедура может осуществляться на разных стадиях, и в идеале способствует восстановлению и ремиелинизации нейронов и аксонов путем создания благоприятной микросреды или непосредственно физического замещения клеток. Необходимый эффект достигается путем подавления воспалительного каскада, возникающего из-за некроза и утраты клеток.
Эмбриональные стволовые клетки - плюрипонтенстные клетки, полученные из внутренней клеточной массы эмбриона, рассматриваются в качестве варианта терапии при ПСМ. Несмотря на то, что эти клетки могут бесконечно делиться и обладают большей способностью к дифференциации, чем региональные (зрелые) стволовые клетки, их использование вызывает множество споров. Китайскому хирургу был предъявлен судебный иск за лечение нескольких сотен пациентов с ПСМ без осложнений путем инъекций обкладочных нейроэпителиальных клеток, выделенных из абортивного материала. Этот случай вызвал волну острых дискуссий об этической стороне подобных исследований.
Компания Gevron Corporation первой в США получила одобрение на клиническое исследование по оценке эффективности эмбриональных стволовых клеток человека в лечении тяжелых повреждениях спинного мозга. Зрелые стволовые клетки чаще, чем эмбриональные используются в экспериментах как in vitro, так и in vivo, именно в связи с этическим вопросом.
Мезенхимальные стволовые клетки (МСК) широко применяются в исследованиях из-за простоты в их получении, изоляции, размножении и хранении. До сих пор не поступало сообщений об иммунологических реакциях у человека на аллогенные трансплантаты по сравнению с аутологичными, что позволяет применять МСК в клеточной терапии. В ходе исследований была продемонстрирована способность МСК стимулировать регенерацию аксонов и подавлять процесс демиелинизации. В ряде различных исследований на крысах было обнаружено, что МСК способствуют регенерации нервов, регулируют производство воспалительных цитокинов, включая TNF-α и IL-6, а также снижают активность миелопероксидазы.
Менезес с коллегами вывели гипотезу, что ламинин может играть решающую роль в сохранении и восстановлении нейронов и аксонов после того, как обнаружили отложения гликопротеина в пораженной области в экспериментальной модели ПСМ у крыс. Результаты всех исследований указывают на то, что действие трансплантированных МСК направлено главным образом на создание благоприятной микросреды путем урегулирования секреции ряда нейротрофических факторов. Тем не менее, дифференциация МСК in vivo в нейрон-подобные клетки является неэффективной. Таким образом, МСК в настоящее время не способны к прямой репопуляции и физическому восстановлению поврежденных тканей при ПСМ.
Нейральные стволовые клетки (НСК) рассматриваются в качестве варианта лечения по причине их способности преодолевать эти недостатки. НСК, полученные из субвентрикулярной зоны способны к дифференциации в нейроны, олигодендроциты и чаще всего – астроциты. Немати с коллегами обнаружили, что трансплантация НСК при закрытых ПСМ у обезьян способствует восстановлению функций тазовых конечностей. В своем исследовании Ли с коллегами также зарегистрировали функциональное восстановление тазовых конечностей, уменьшение повреждений, а также увеличение плотности аксонов и дендритных шипиков вокруг пересаженных НСК у крыс. Пилти с коллегами оценивали частоту выживаемости, миграцию и разрастание (спраутинг) сенсорных волокон трансплантированных НСК у крыс во вторичной или подострой стадии по сравнению с третичной или хронической стадии ПСМ. Исследователи обнаружили, что меньшее количество трансплантированных клеток прижилось в группе, проходившей лечение на третичной стадии ПСМ, однако эти клетки сильно увеличивали популяцию зрелых олигодендроцитов.
Экспериментальное применение стволовых клеток для лечения ПСМ в настоящее времени весьма ограничено. По результатам нескольких исследований выявлены улучшения сенсорных и моторных показателей спустя 1-3 месяцев после трансплантации с использованием других клеток и факторов роста. Исследователь Карамоузин с коллегами утверждают, что несмотря на доступность и безопасность клеточной трансплантации, положительные сдвиги в функциональном восстановление не были статистически значимыми. Из-за небольшой популяции участников исследований, затруднительно с точностью заявлять о клинической эффективности трансплантации стволовых клеток при ПСМ.
Дополнительные сферы интересов, которые не рассматривались с точки зрения трансплантации стволовых клеток, это ятрогенные повреждения нервов и мускулов при ПСМ. Дополнительными факторами, которые необходимо принимать во внимание, является этический вопрос и канцерогенный риск при использовании эмбриональных стволовых клеток, возможная иммунная реакция на аутологичные трансплантаты, а также клиническая заболеваемость при отборе взрослых стволовых клеток. В целом, стандартизация экспериментов in vitro и на животных моделях может ускорить перевод трансплантации стволовых клеток от исследований в клиническую практику для нужд спинальной хирургии.
Заболевания
Грыжа межпозвоночного диска
Миелопатия
Спондилолистез
Стеноз позвоночного канала
Процедуры
Декомпрессия нерва
Дискэктомия
Ламинопластика
Ламинэктомия
Регенеративная медицина в ортопедической хирургии
Спондилодез
Фораминотомия